Neuromodulação na Doença de Parkinson: quando considerar marca-passo cerebral, o que esperar e onde entram outras técnicas
Publicado em 21 de abril de 2026
O DBS (estimulação cerebral profunda) é uma ferramenta potente para o Parkinson avançado, mas depende de indicação precisa. Entenda o que o marca-passo cerebral realmente pode fazer pela sua qualidade de vida.


Dr. Thiago G. Guimarães
CRM-SP 178.347 | RQE 83752
Neurologista formado pela USP, especialista em Distúrbios do Movimento e Neurogenética. Corpo clínico do Hospital Sírio-Libanês e Hospital Albert Einstein.
Neuromodulação na Doença de Parkinson: quando considerar marca-passo cerebral, o que esperar e onde entram outras técnicas
A Doença de Parkinson não é apenas uma doença do tremor. Com a progressão, muitos pacientes passam a enfrentar um problema mais difícil: os remédios ainda ajudam, mas o efeito fica curto, irregular ou acompanhado de discinesias. É nessa fase que a conversa sobre neuromodulação ganha importância.
Entre as formas de neuromodulação, a estimulação cerebral profunda — conhecida como DBS, ou “marca-passo cerebral” — é hoje uma das terapias mais consolidadas para pacientes com Parkinson avançado e complicações motoras refratárias ao ajuste medicamentoso. O DBS consiste na implantação de eletrodos em alvos profundos do cérebro, conectados a um gerador implantável, que fornece estimulação elétrica contínua e ajustável.
Mas há um ponto decisivo: DBS não é “cura” do Parkinson, não serve para todos os pacientes e não melhora todos os sintomas da doença. O maior erro é pensar nessa cirurgia como uma solução geral. O melhor jeito de entendê-la é como uma ferramenta de modulação de circuitos — muito potente, mas dependente de indicação correta, alvo correto e programação correta.
O que é neuromodulação no Parkinson
Neuromodulação é o uso de estímulos elétricos ou magnéticos para alterar a atividade de circuitos cerebrais. No Parkinson, isso interessa porque a doença produz padrões anormais de funcionamento nos circuitos dos gânglios da base, especialmente relacionados a lentidão, rigidez, tremor e flutuações motoras. Em vez de “dar energia” ao cérebro, como em algumas metáforas didáticas, o objetivo real é reorganizar a atividade desses circuitos de forma mais fisiológica.
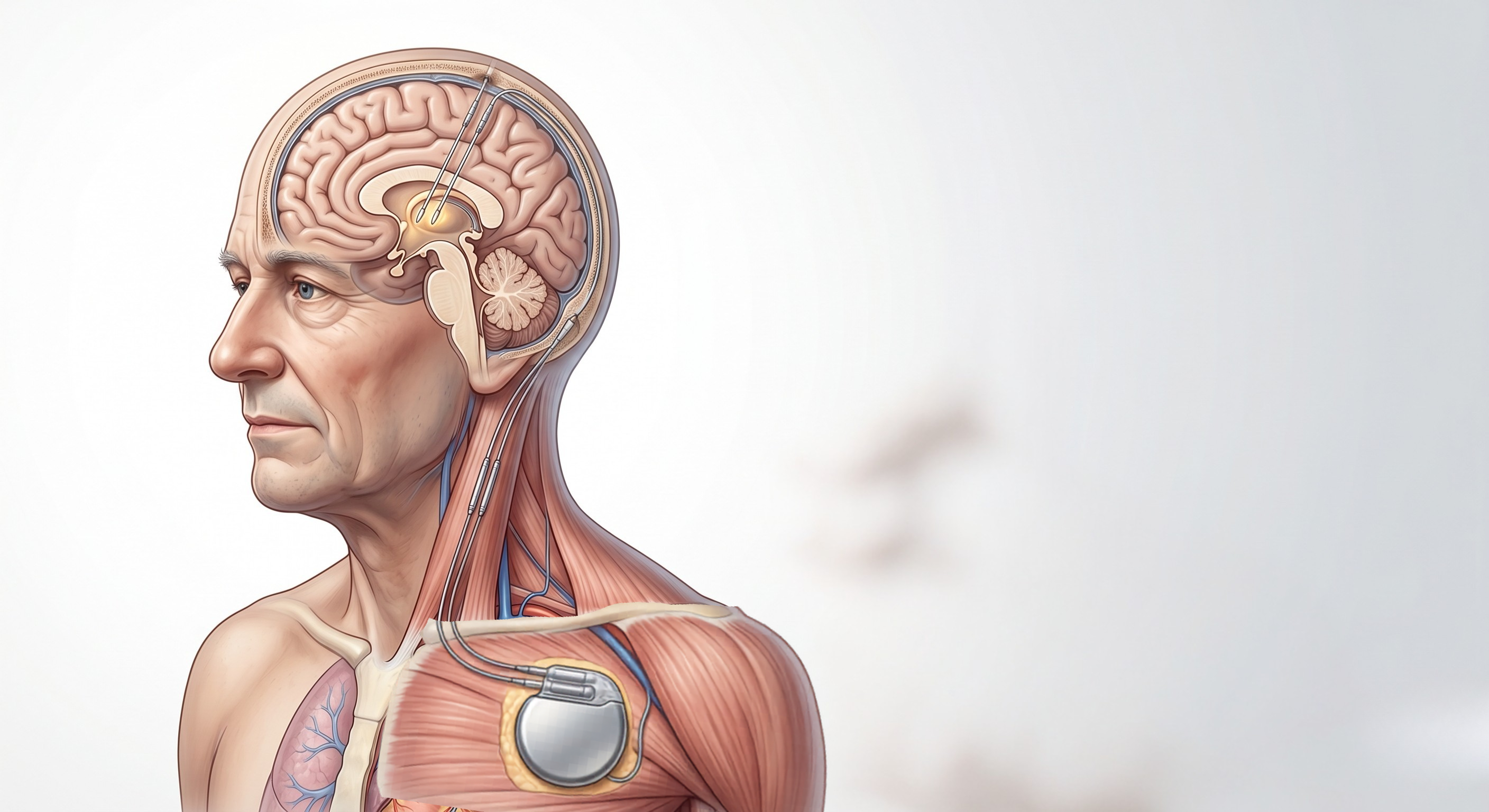
Essa distinção importa. Dizer que existe uma “área sem energia” ajuda a explicar para o leigo, mas é incompleto. O que a literatura moderna descreve é uma modulação de rede: o DBS interfere em padrões patológicos de atividade neural e pode reduzir a sincronização anormal associada ao comprometimento motor.
Quando o remédio começa a “não durar”
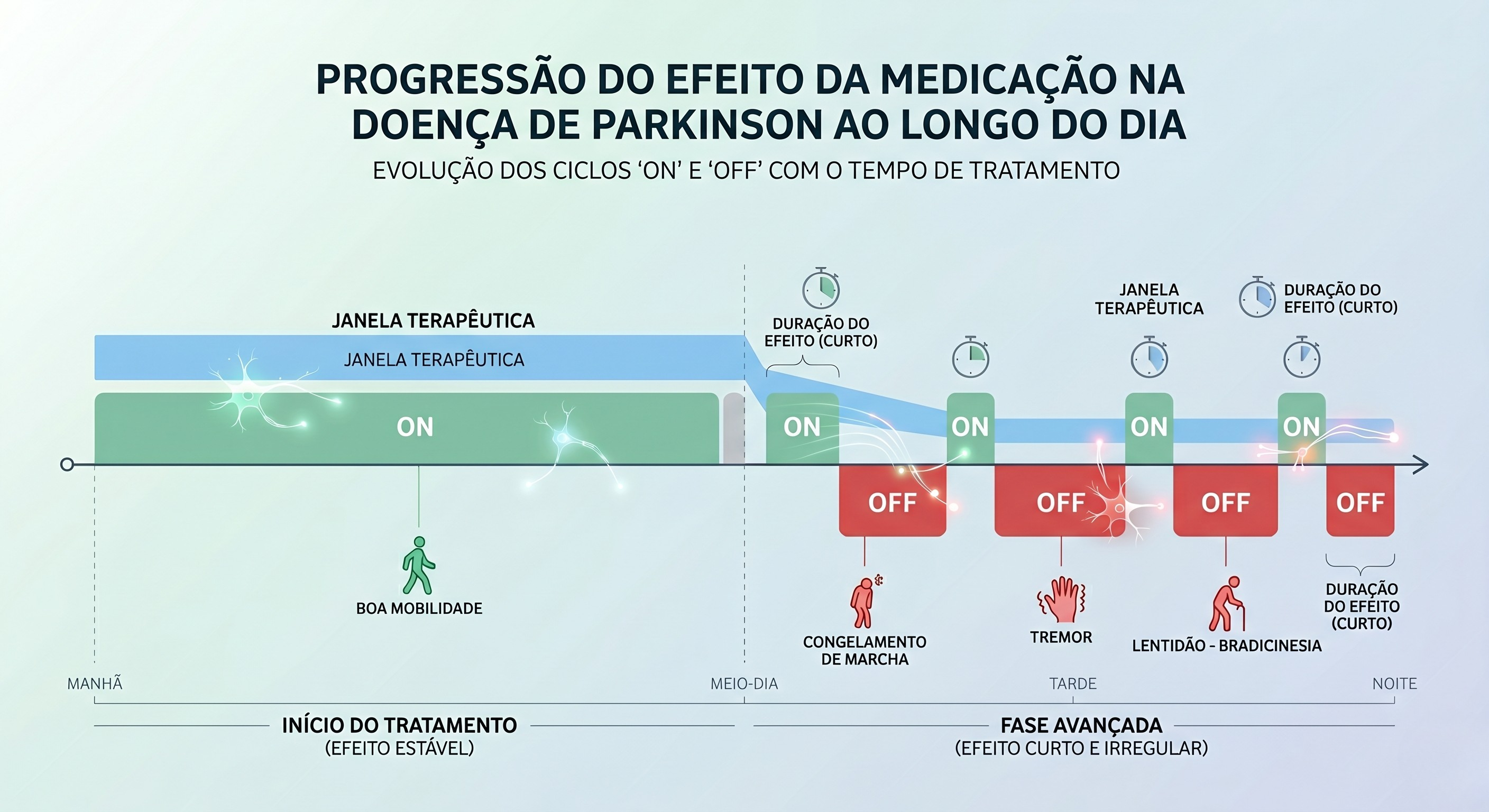
Muitos pacientes reconhecem esse momento antes mesmo de saber nomeá-lo. A medicação ainda funciona, mas o corpo entra em “modo OFF” antes da próxima dose. Em outros casos, o paciente melhora com a levodopa, mas paga o preço com movimentos involuntários, as discinesias.
Esse é exatamente o cenário clássico em que o DBS passa a ser discutido: flutuações motoras importantes, períodos OFF incapacitantes e discinesias problemáticas, apesar de tratamento clínico otimizado.
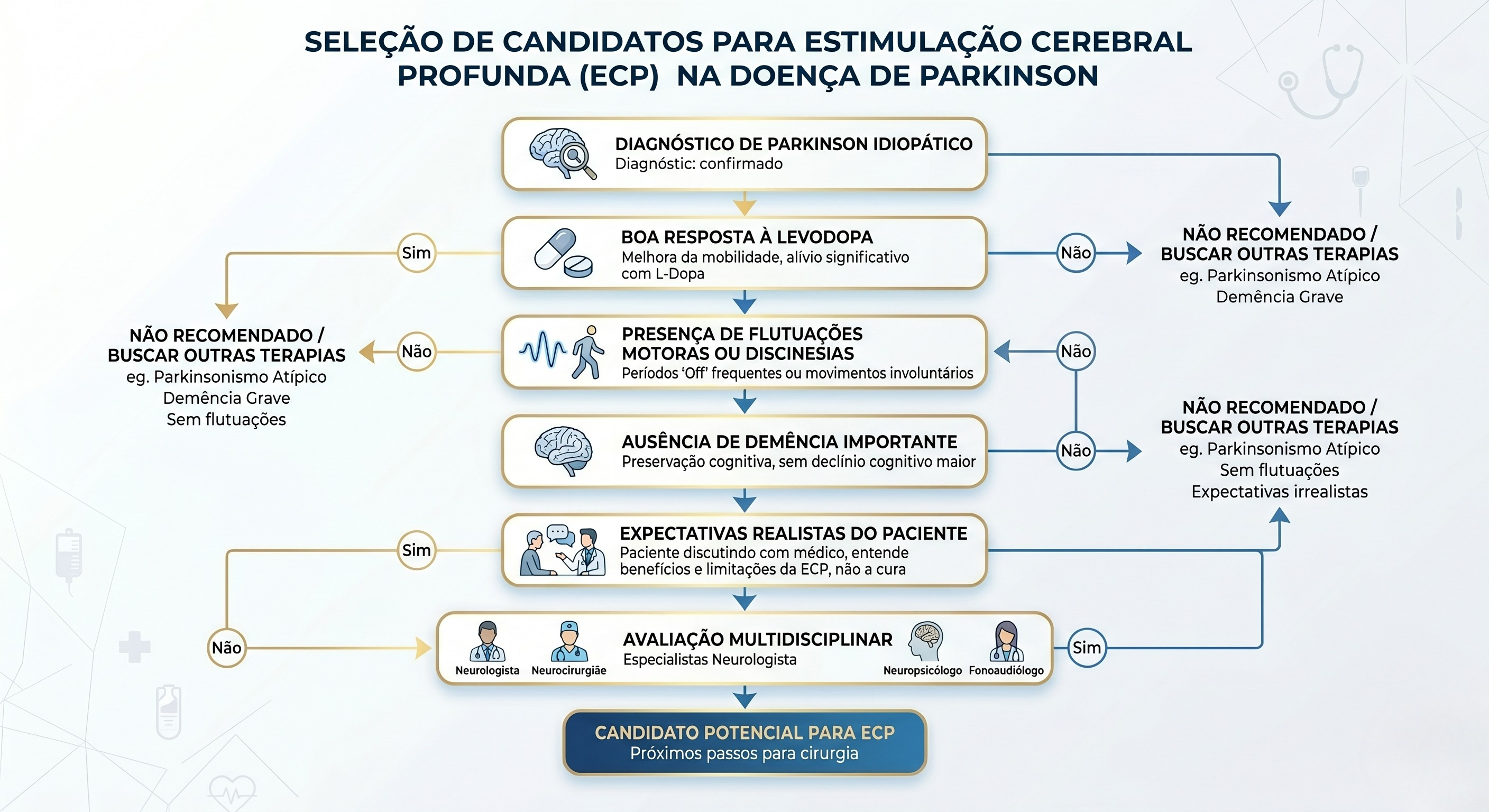
Quem costuma ser um bom candidato para DBS
De forma geral, o melhor candidato é o paciente com Doença de Parkinson idiopática, evolução compatível, boa resposta prévia à levodopa e complicações motoras relevantes que já não estão sendo controladas de forma satisfatória apenas com remédios.
O princípio mais útil é simples: o DBS tende a melhorar principalmente aquilo que também melhora com levodopa. Isso inclui, em especial, bradicinesia, rigidez e tremor responsivo à dopamina. Há duas exceções clínicas importantes: o tremor pode às vezes responder ao DBS mesmo quando é pouco responsivo à levodopa, e as discinesias podem melhorar muito após a cirurgia, dependendo do alvo escolhido.
Por outro lado, alguns problemas respondem mal ao DBS ou podem até piorar: demência, instabilidade postural grave com quedas frequentes, fala já muito comprometida, disfagia avançada e sintomas axiais pouco responsivos à dopamina. Nesses contextos, a cirurgia precisa ser discutida com cautela.
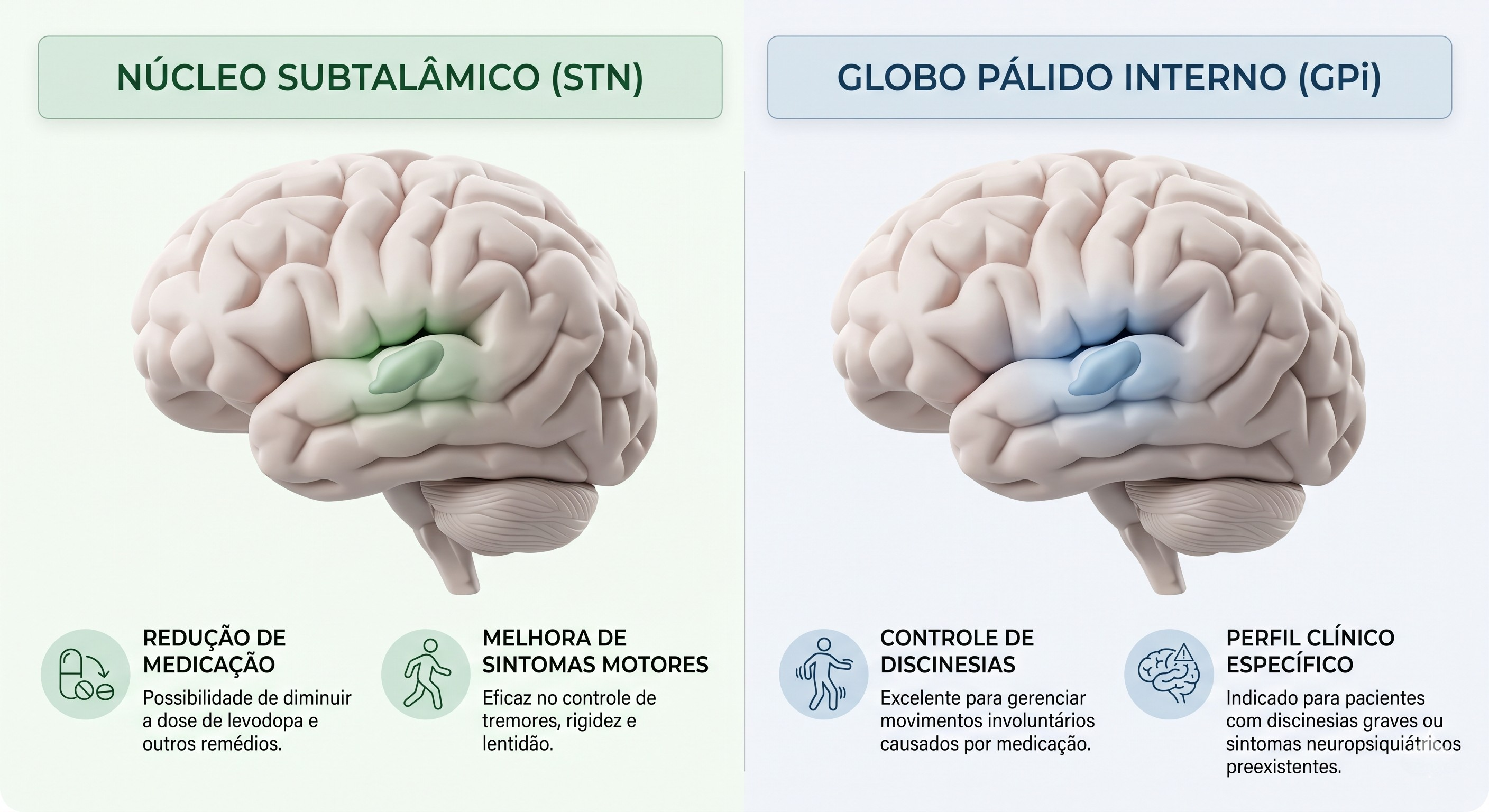
STN ou GPi: por que o alvo faz diferença
Para Parkinson, os dois alvos mais usados são o núcleo subtalâmico, o STN, e o globo pálido interno, o GPi. Os dois podem melhorar tremor, rigidez e bradicinesia, mas não são equivalentes em tudo.
O STN costuma ser preferido quando se deseja maior redução de carga medicamentosa. Isso pode ser muito útil em pacientes com flutuações motoras e necessidade de doses altas ou frequentes de levodopa. Parte do benefício sobre discinesias no STN vem justamente desse efeito poupador de medicação.
O GPi, por sua vez, tem um perfil muito atraente quando a discinesia é o principal problema. Nesse alvo, existe um efeito antidiscinético mais direto, menos dependente da redução de remédio. Além disso, em alguns pacientes com maior vulnerabilidade cognitiva ou psiquiátrica, o GPi pode ser uma escolha mais confortável.
Em outras palavras: não existe “melhor alvo” universal. Existe o alvo mais coerente para aquele fenótipo clínico.
O que o DBS melhora — e o que ele não promete
Quando bem indicado, o DBS pode reduzir tremor, rigidez, bradicinesia, tempo em OFF e discinesias, além de melhorar qualidade de vida e previsibilidade do estado motor.
Mas é igualmente importante dizer o que ele não promete. O DBS não reverte a progressão neurodegenerativa, não costuma corrigir constipação, não é tratamento primário de memória, não resolve automaticamente problemas urinários e não transforma sintomas axiais avançados em sintomas leves. Isso precisa ficar explícito desde a primeira conversa. O resultado bom em DBS depende tanto da técnica quanto de expectativa realista.
A cirurgia é só metade do tratamento
Um dos pontos mais subestimados pelo público é que a cirurgia não encerra o processo. Depois do implante, começa uma fase longa de programação. A literatura de revisão deixa claro que programação ainda é um processo manual, complexo, muito dependente de experiência clínica, e que frequentemente exige várias visitas ao longo dos primeiros 6 a 12 meses até estabilizar parâmetros e medicação.

Na prática, a equipe procura o melhor contato, a melhor amplitude, largura de pulso e frequência, sempre tentando ampliar a janela terapêutica: máximo benefício com mínimo efeito adverso. Tremor e rigidez costumam responder rápido; bradicinesia pode demorar mais para ser julgada com segurança.
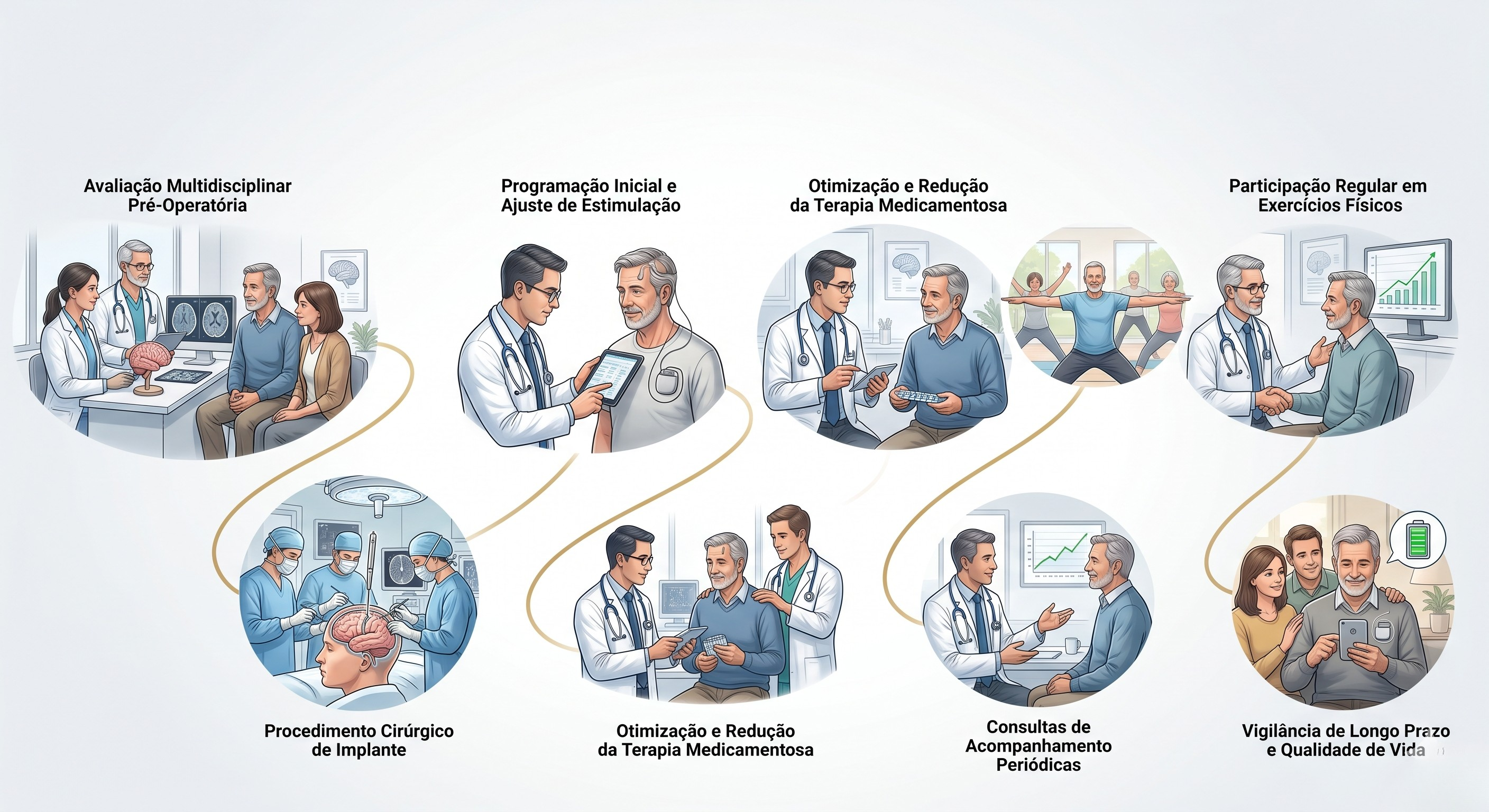
É por isso que a frase “operei e não melhorei” quase nunca deve encerrar a discussão. Antes disso, é preciso revisar pelo menos quatro grupos de problemas: indicação inadequada, posição do eletrodo, programação subótima e ajuste medicamentoso mal calibrado. O seu material visual capta isso muito bem; o artigo só precisa dizer isso com menos tom de sentença e mais tom de investigação clínica.
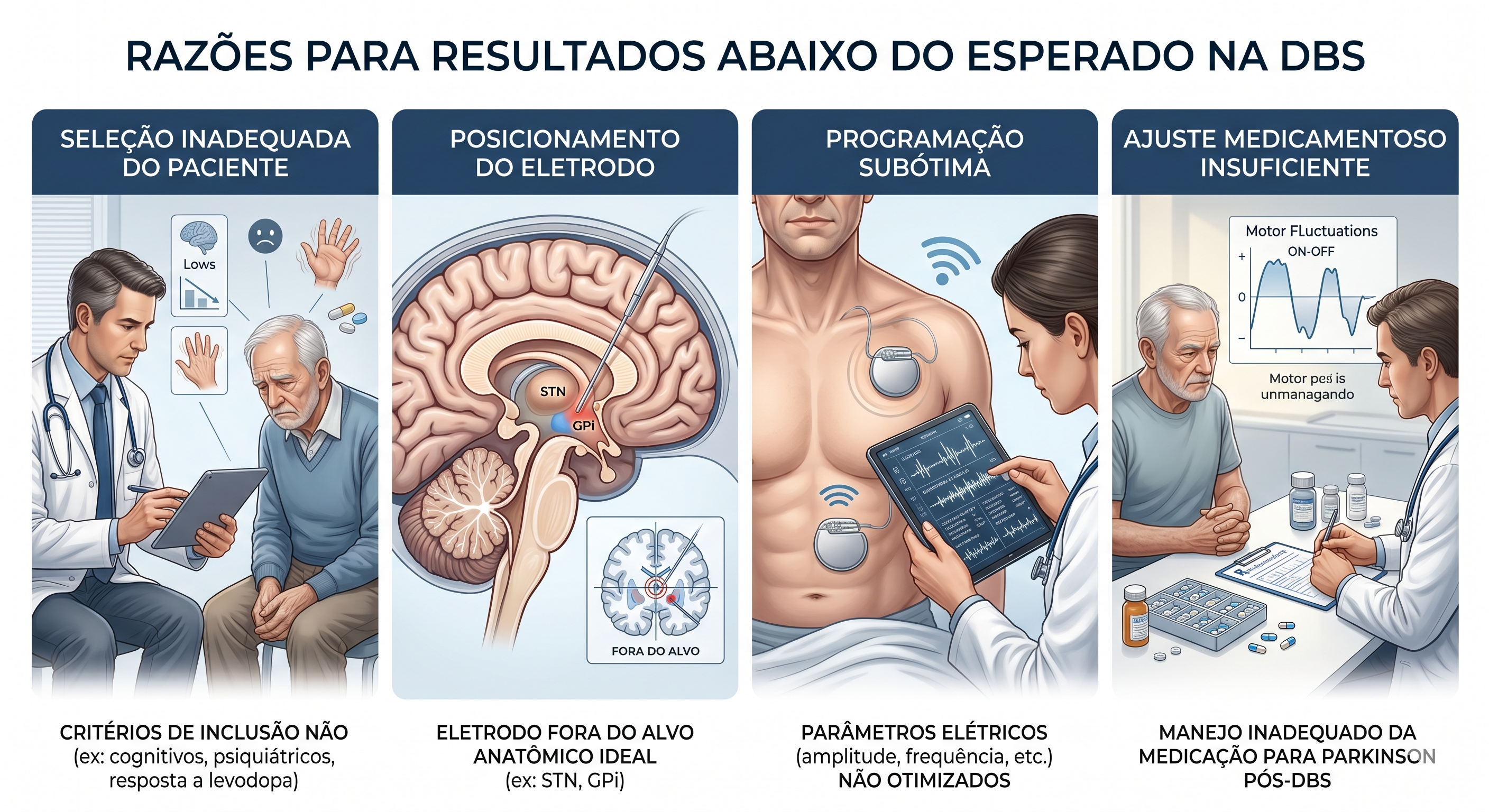
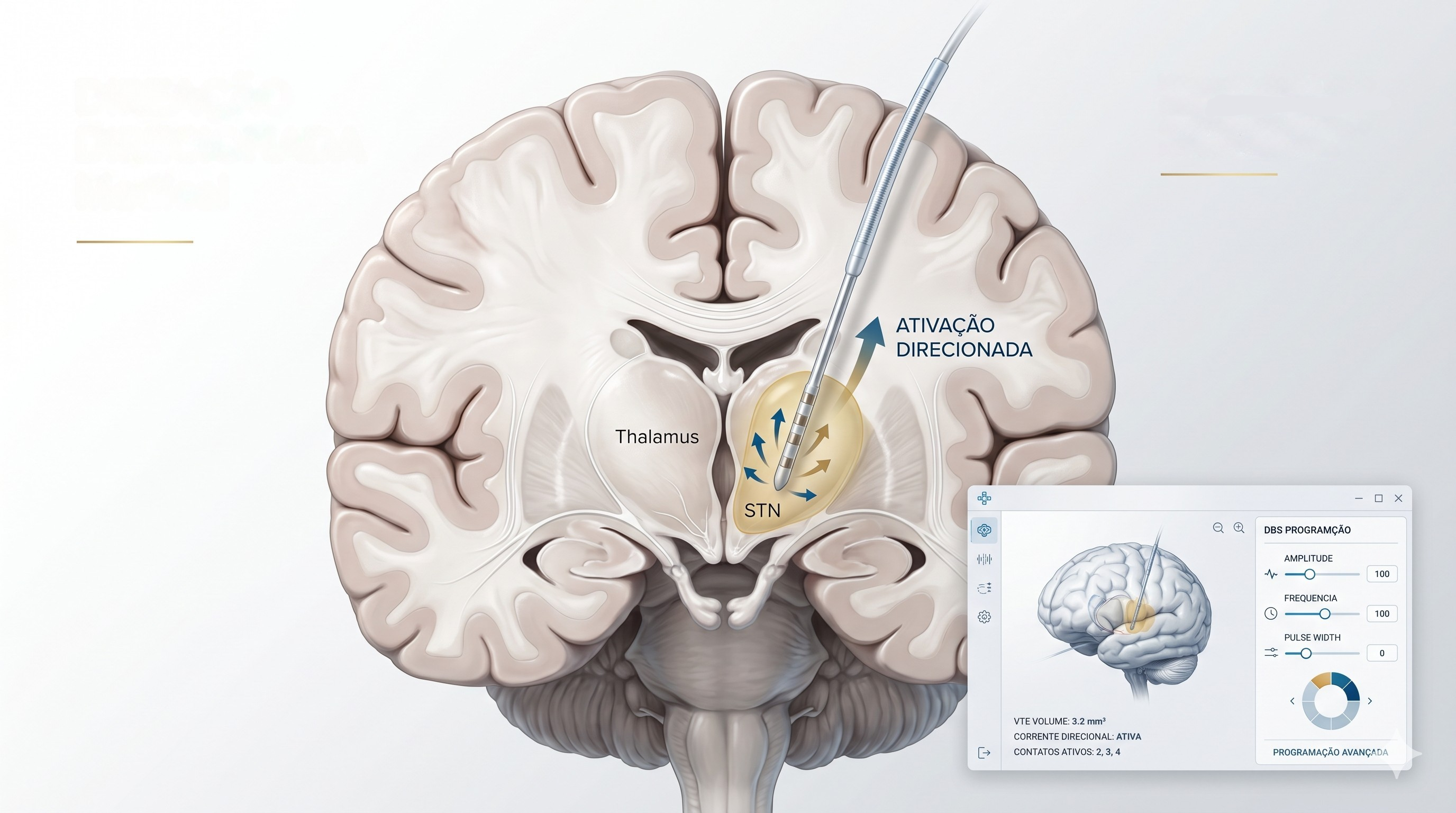
Onde entram os eletrodos direcionais, a imagem e a programação avançada
A programação atual está mudando. Eletrodos direcionais permitem “empurrar” o campo elétrico para um lado e afastá-lo de estruturas relacionadas a efeitos colaterais. Isso amplia a margem terapêutica e melhora a precisão do ajuste.
Além disso, softwares de visualização tridimensional e programação guiada por imagem já estão sendo incorporados à prática, reduzindo tempo de programação e ajudando a correlacionar sintomas, anatomia e campo estimulado. Revisões recentes citam GUIDE XT e ferramentas semelhantes como parte dessa tendência.
O próximo passo é o DBS adaptativo. Em vez de estimular de forma fixa o tempo todo, sistemas adaptativos usam sinais neurais para ajustar a estimulação em tempo real. Em um ensaio randomizado de viabilidade, o aDBS reduziu o tempo passado com sintomas motores incômodos em comparação ao DBS convencional otimizado e melhorou qualidade de vida em parte dos pacientes, embora ainda estejamos falando de amostra pequena e tecnologia em consolidação.
E o TMS?
A estimulação magnética transcraniana, ou TMS, é uma forma não invasiva de neuromodulação. Ela não substitui o DBS em pacientes com flutuações motoras graves e indicação cirúrgica clássica. O papel dela é diferente.
Em vez de agir em um alvo profundo com estimulação contínua, o TMS atua mais superficialmente, em sessões repetidas, e pode ser pensado como ferramenta adjunta em contextos específicos de reabilitação, marcha ou modulação cortical. Não é razoável apresentá-lo como “concorrente direto” do DBS em doença de Parkinson avançada.
Vida depois do marca-passo cerebral
O pós-operatório de longo prazo também precisa ser explicado com clareza. O paciente passa a conviver com um sistema implantado, o que exige seguimento, checagem de bateria, proteção da loja do gerador e atenção a compatibilidades específicas com exames e fontes magnéticas, dependendo do dispositivo. Além disso, cirurgia boa sem reabilitação, atividade física e ajuste clínico continuado entrega menos do que poderia. A cirurgia é o começo de uma nova fase, não o ponto final.

O que este texto quer deixar claro
Neuromodulação no Parkinson não é uma disputa entre “remédio ou cirurgia”. É uma mudança de estratégia quando a doença entra em uma fase em que a resposta clínica passa a depender não apenas do fármaco, mas também da capacidade de modular circuitos de forma estável, personalizada e sustentável.
O DBS é hoje a forma mais potente e consolidada de fazer isso em pacientes bem selecionados. Mas potência sem indicação correta vira frustração. O melhor resultado vem quando três coisas andam juntas: diagnóstico certo, alvo certo e programação certa.
O que este artigo NÃO prova
Este artigo não prova que todo paciente com Parkinson avançado deve operar. Também não prova que STN seja sempre melhor que GPi, nem que TMS tenha papel equivalente ao DBS. E não prova que tecnologias mais novas, como DBS adaptativo ou programação conectômica, já sejam padrão para todos os serviços. O que a evidência atual sugere é outra coisa: o campo está migrando de uma neuromodulação “estática” para uma neuromodulação cada vez mais personalizada, guiada por anatomia, fisiologia e perfil clínico.
Artigos Relacionados
Selecionamos outros conteúdos sobre o mesmo tema para aprofundar a leitura de forma prática e organizada.

Movimentos paroxísticos: quando crises de distonia, coreia ou ataxia aparecem de repente
Entenda o que são distúrbios do movimento paroxísticos, como eles aparecem, quais causas precisam ser investigadas e por que genética, epilepsia e exames podem fazer diferença no tratamento.

Demência com Corpos de Lewy: o que os sintomas revelam sobre o futuro
A demência com corpos de Lewy tem sinais específicos que ajudam médicos e famílias a prever o curso da doença. Saber reconhecê-los faz diferença no cuidado e no planejamento.
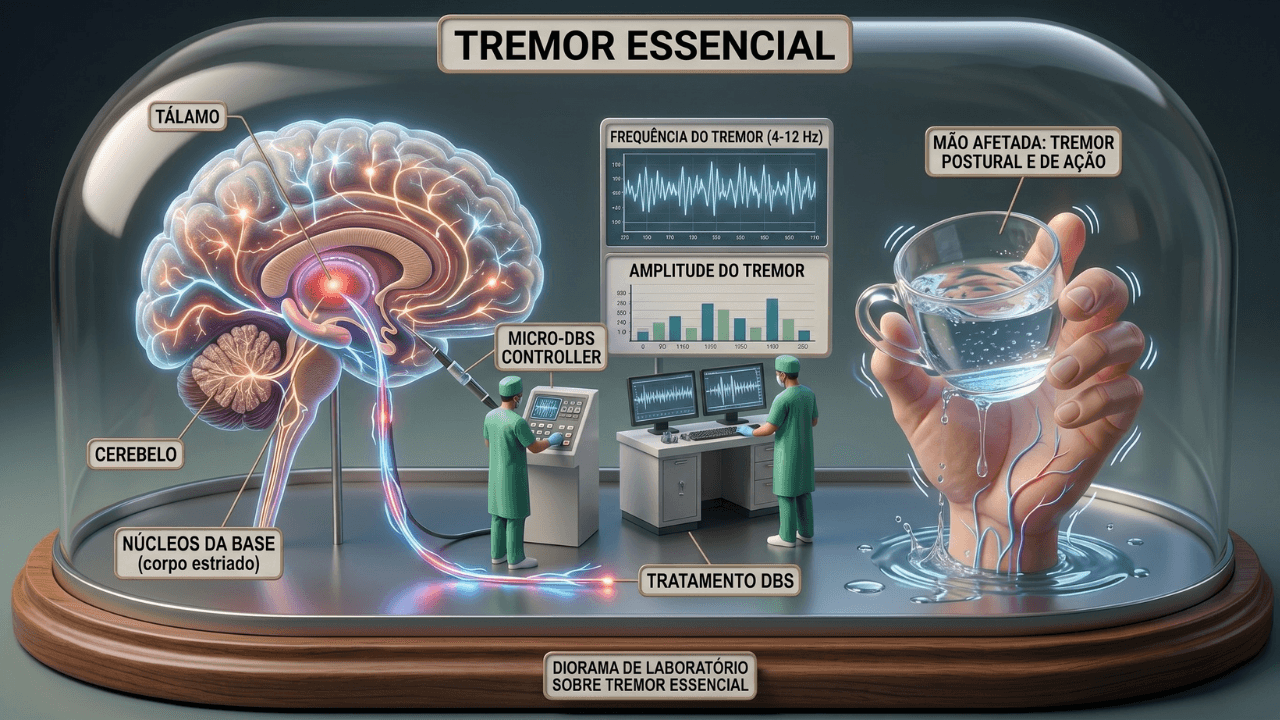
Tremor essencial: o que mudou entre os reviews da MDS de 2019 e 2026 sobre os remédios
Os reviews da MDS de 2019 e 2026 sobre tremor essencial chegam a uma mensagem importante: alguns remédios continuam sendo usados na prática, mas a confiança científica neles ficou mais cautelosa quando a análise metodológica ficou mais rigorosa.

Levodopa no Parkinson: o que a resposta ao remédio realmente significa?
Entenda, em linguagem simples, o que a resposta à levodopa pode indicar no Parkinson, na atrofia de múltiplos sistemas e na paralisia supranuclear progressiva.
Agende sua Consulta
Discuta seu caso com o Dr. Thiago G. Guimarães, neurologista formado pela USP, especialista em Distúrbios do Movimento e Neurogenética. Atendimento presencial em São Paulo ou por telemedicina.
📍 Consultório: R. Cristiano Viana, 328 - Conj. 201, Pinheiros, São Paulo/SP