Síndrome MELAS: quando o cérebro fica sem energia — diagnóstico, genética e tratamentos
MELAS é uma doença genética rara causada por defeito no DNA das mitocôndrias — as usinas de energia das células — que provoca crises cerebrais parecidas com AVC, especialmente em jovens. Hoje existem tratamentos que reduzem significativamente a frequência dessas crises.
Publicado em 12 de maio de 2026
MELAS é uma doença rara do DNA mitocondrial que imita um AVC, mas tem causas e tratamentos completamente diferentes. Saiba como ela é diagnosticada, quem corre risco e quais tratamentos funcionam.

Dr. Thiago G. Guimarães
CRM-SP 178.347 | RQE 83752
Neurologista formado pela USP, especialista em Distúrbios do Movimento e Neurogenética. Corpo clínico do Hospital Sírio-Libanês e Hospital Albert Einstein.
Síndrome MELAS: quando o cérebro fica sem energia — diagnóstico, genética e tratamentos
MELAS não é AVC — e essa diferença pode ser decisiva
Se alguém da sua família teve o que pareceu um AVC ainda jovem — com confusão mental, perda de visão ou fraqueza súbita — mas os exames convencionais não encontraram nenhum vaso entupido, existe uma possibilidade que poucos médicos fora de centros especializados consideram: a síndrome MELAS.
MELAS é uma doença rara das mitocôndrias, as "usinas de energia" das células. Quando essas usinas falham, o cérebro sofre crises que imitam AVCs com surpreendente precisão — mas têm causa, mecanismo e tratamento completamente diferentes. Tratar um episódio de MELAS como AVC comum pode ser não apenas ineficaz, mas potencialmente perigoso.
Este guia reúne o que há de mais atual em cinco estudos científicos publicados entre 2020 e 2024 para responder, em linguagem direta: o que é MELAS, como ela é reconhecida, quem corre risco de tê-la e quais tratamentos funcionam.
Em 30 segundos
- O tema: MELAS é uma síndrome mitocondrial genética rara que causa crises cerebrais parecidas com AVCs, especialmente em jovens.
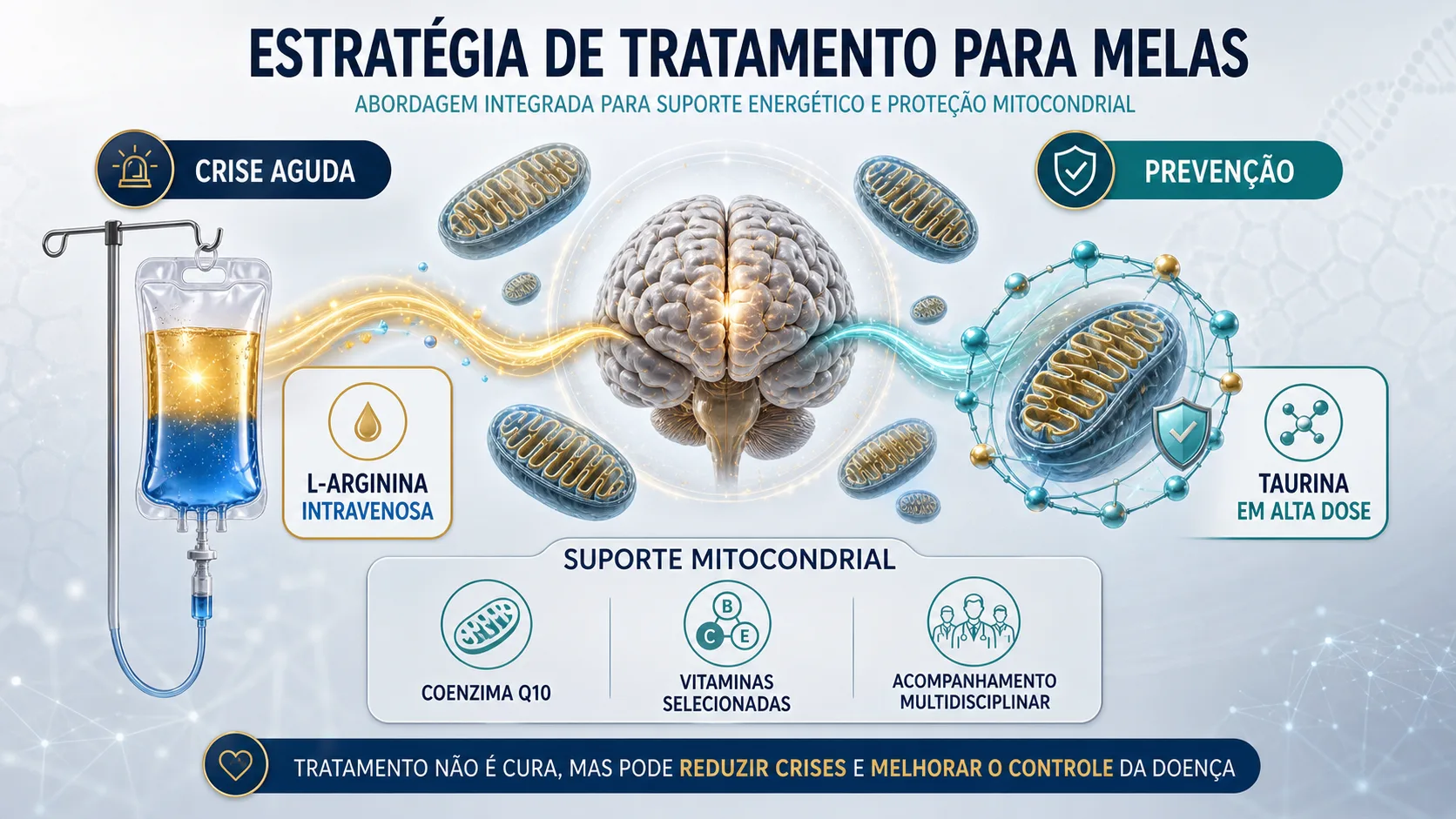
- O achado central: tratamentos como taurina em alta dose e L-arginina intravenosa reduzem significativamente a frequência e gravidade das crises — mas ainda não existe cura.
- Para quem serve: pessoas com diagnóstico de MELAS, familiares, portadores da mutação e médicos que acompanham esses pacientes.
- O principal limite: a maioria dos tratamentos ainda é baseada em estudos pequenos e consenso de especialistas, não em grandes ensaios clínicos controlados.
O que importa de verdade
A MELAS não é um AVC — e o tratamento do AVC não funciona aqui. Por que importa: a trombolise (tratamento padrão do AVC) pode ser inadequada em MELAS. O diagnóstico correto na urgência é literalmente vital. A nuance: clínicos não especializados costumam não considerar MELAS por desconhecimento — leve sempre um cartão de identificação com o diagnóstico.
O exame de sangue pode dar falso negativo. Por que importa: a mutação pode estar "escondida" no músculo ou na urina, com proporção baixa no sangue. Um resultado negativo não exclui o diagnóstico quando a suspeita clínica é forte. A nuance: exige que o médico conheça essa limitação e solicite testes em outros tecidos.
Dois perfis de MELAS existem — com prognósticos diferentes. Por que importa: a forma clássica (início após os 10 anos, mutação m.3243A>G) evolui mais lentamente; a forma atípica (início na infância, outras mutações) tende a ser mais agressiva. A nuance: reconhecer o perfil ajuda a antecipar complicações e planejar o acompanhamento.
Hoje há tratamentos que realmente reduzem as crises. Por que importa: 60% dos pacientes em um ensaio clínico Fase III ficaram completamente sem crises com taurina em alta dose por um ano. L-arginina intravenosa melhora os sintomas agudos na maioria dos casos. A nuance: esses são estudos pequenos — os resultados são encorajadores, mas precisam de confirmação em escalas maiores.
A hereditariedade é materna — mas não é destino. Por que importa: todos os filhos de uma mãe afetada herdam a mutação, mas nem todos desenvolvem a doença completa. A nuance: a gravidade depende de quantas mitocôndrias com defeito cada pessoa herda — e isso varia muito dentro da mesma família.
Para quem este texto é útil
Este artigo é especialmente útil para pessoas que receberam o diagnóstico de MELAS ou têm familiar diagnosticado, portadores da mutação m.3243A>G ainda sem sintomas, e famílias que buscam entender a hereditariedade e o risco para outros membros. Também pode ajudar quem está no processo de investigação diagnóstica — aqueles casos em que "parece AVC mas não é" ficam sem explicação por anos.
O que é MELAS, em linguagem simples?
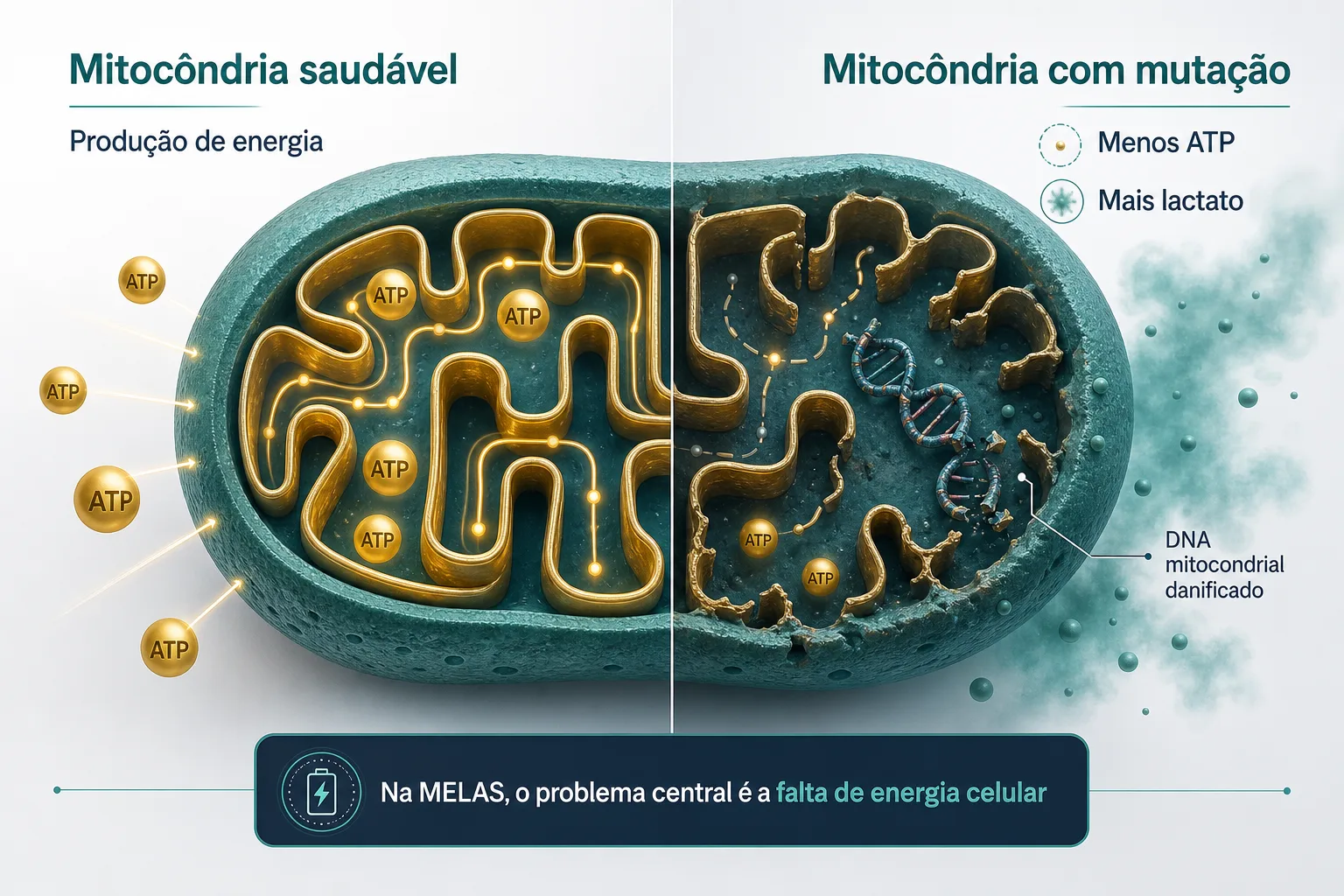
Mitocôndrias são estruturas dentro de cada célula do nosso corpo responsáveis por transformar o oxigênio e os alimentos em energia utilizável — o ATP, o "combustível" celular. Pense nelas como usinas de energia de um bairro.
Em MELAS, uma alteração no DNA dessas usinas faz com que a produção de energia seja deficiente. Quando a demanda energética é alta — como no cérebro durante uma crise — as usinas não conseguem suprir a demanda. O resultado é um "apagão localizado" no cérebro: a área afetada para de funcionar temporariamente, causando os sintomas que imitam um AVC.
A sigla MELAS vem do inglês: Mitochondrial Encephalomyopathy (encefalopatia e miopatia mitocondriais), Lactic Acidosis (acidose lática) e Stroke-like Episodes (episódios tipo AVC).
A analogia mais útil: imagine que o seu cérebro é uma cidade que precisa de energia constante. As usinas (mitocôndrias) têm um defeito de fabricação em algumas unidades. Enquanto as unidades funcionais suprem a demanda, tudo funciona bem. Quando o número de unidades com defeito ultrapassa certo limite num bairro específico — o bairro apaga.
Como o MELAS aparece no dia a dia?
O primeiro sinal de MELAS frequentemente acontece assim: uma pessoa jovem — adolescente ou adulto jovem — acorda com uma dor de cabeça intensa, diferente das anteriores. Em seguida, começa a ver mal de um lado, ou percebe que uma parte do campo visual sumiu. Talvez tenha uma convulsão. Na chegada ao pronto-socorro, a ressonância magnética mostra uma "mancha" no cérebro — e o médico de plantão suspeita de AVC.
Semanas depois, a "mancha" desaparece. Mas alguns meses mais tarde, outra aparece do outro lado. Esse padrão migratório — lesões que aparecem, somem e reaparecem em outros locais — é uma das características mais específicas da MELAS.
Além dos episódios cerebrais, MELAS pode se manifestar como fadiga intensa e desproporcional ao esforço, surdez que piora progressivamente (geralmente bilateral, sensorioneural), baixa estatura, diabetes de início precoce (diferente do tipo 2 comum), fraqueza muscular, cefaleia frequente do tipo enxaqueca e comprometimento gradual da memória e raciocínio.
O que os estudos pesquisaram?
Esta análise integra cinco publicações científicas complementares.
- Na & Lee (2024), publicada na revista Biomolecules, revisou o estado atual do diagnóstico e tratamento da MELAS, com destaque para fisiopatologia e terapias emergentes.
- Barcelos et al. (2020), publicada no Current Opinion in Pediatrics, forneceu as diretrizes mais atuais de dosagem dos suplementos e medicamentos mitocondriais.
- Alves et al. (2023), publicada no AJNR, analisou 35 pacientes com MELAS confirmado geneticamente e identificou dois fenótipos distintos por análise de agrupamento não supervisionado.
- Seed et al. (2022), publicada no Molecular Genetics & Genomic Medicine, revisou 114 casos pediátricos da literatura e apresentou três casos próprios de Cambridge.
- Tetsuka et al. (2021), publicada no Metabolic Brain Disease, detalhou os mecanismos dos episódios tipo AVC e os tratamentos mais recentes.
Tipo de evidência predominante: revisões narrativas de qualidade, um estudo de fenótipo retrospectivo e uma série de casos com revisão sistemática. O nível de evidência é moderado — ainda há escassez de grandes ensaios clínicos randomizados nessa área.
O que foi descoberto?
Quão comum é a MELAS?
MELAS não é tão rara quanto parece. As doenças mitocondriais primárias afetam pelo menos 1 em cada 4.300 pessoas. A mutação mais comum associada à MELAS — chamada m.3243A>G — está presente em ao menos 3,5 em cada 100.000 pessoas. Muitas dessas pessoas nunca desenvolverão a síndrome completa, porque carregam a mutação em proporção baixa.
A síndrome MELAS propriamente dita tem prevalência de 0,18 por 100.000 pessoas — cerca de 18 casos em 10 milhões. No Brasil, isso representaria aproximadamente 3.800 a 4.000 pessoas com diagnóstico confirmável.
A genética: o que está errado e como é herdado
A causa mais comum de MELAS é uma alteração em apenas uma "letra" do código genético mitocondrial: a mutação m.3243A>G no gene MT-TL1, responsável por aproximadamente 80% dos casos.
Esse gene produz um componente essencial para a síntese de proteínas dentro da mitocôndria — um RNA transportador da leucina. Quando mutado, esse componente não consegue ler corretamente certas instruções do código genético. É como um erro de digitação num manual de instruções que faz a fábrica produzir peças defeituosas. O resultado é que várias proteínas fundamentais para a cadeia de produção de energia não são fabricadas corretamente.
Outras mutações — nos genes MT-ND5, MT-ND1, MT-TH, MT-TK, MT-ATP6 — respondem pelos 20% restantes dos casos e frequentemente produzem variantes clínicas diferentes.
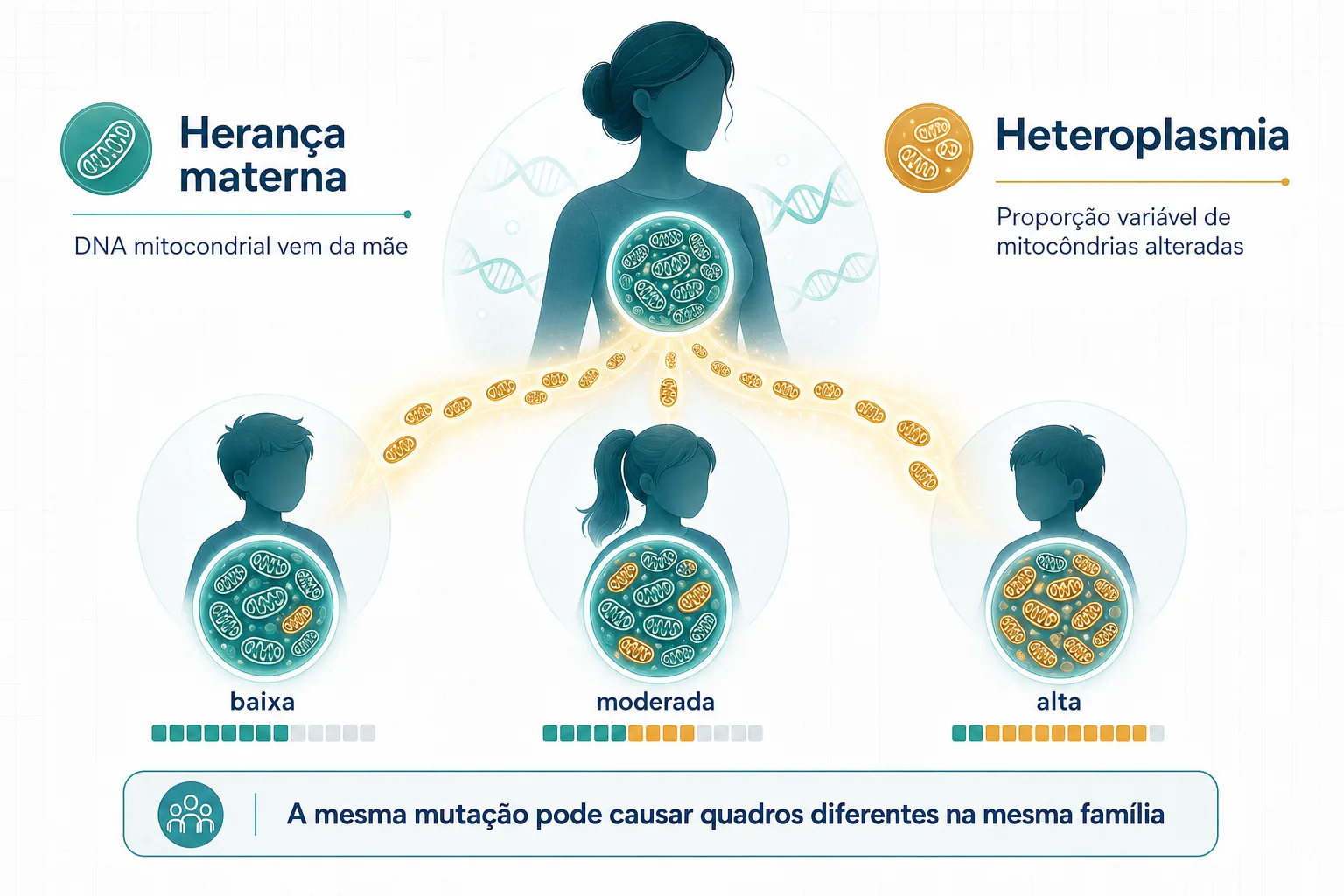
A herança é materna: o DNA mitocondrial vem exclusivamente da mãe, transmitido pelos óvulos. Todos os filhos de uma mãe afetada herdam a mutação. Porém, apenas as filhas transmitem para a próxima geração — os filhos homens não passam a mutação adiante.
O conceito mais importante da genética de MELAS é a heteroplasmia — a mistura de mitocôndrias normais e mutadas dentro de cada célula. A proporção de mitocôndrias mutadas determina a gravidade:
- Proporção de 50–70%: geralmente diabetes e surdez, sem as crises cerebrais.
- Proporção acima de 80%: manifestações neurológicas graves, incluindo os episódios tipo AVC.
Essa proporção varia entre órgãos do mesmo paciente, entre pessoas da mesma família e mesmo ao longo da vida de um indivíduo. É por isso que dois irmãos com a mesma mutação podem ter apresentações clínicas completamente diferentes.
O diagnóstico: onde mora a armadilha
MELAS é frequentemente confundida com AVC por anos. O diagnóstico exige uma combinação de suspeita clínica + exames complementares específicos.
Sinais que devem acender o alerta:
- Episódio "tipo AVC" em pessoa com menos de 40 anos sem fatores de risco cardiovascular clássicos.
- Lesões na ressonância que não correspondem a territórios vasculares definidos.
- Lesões que "migram" entre exames.
- Associação de surdez, cefaleia tipo enxaqueca, diabetes ou baixa estatura na mesma pessoa ou família.
- Mãe com histórico semelhante.
Exames fundamentais:
- Lactato no sangue e no líquor elevados — indicam que as células estão usando vias alternativas de produção de energia, gerando ácido lático como subproduto.
- Teste genético para m.3243A>G no sangue — primeira etapa, alta sensibilidade.
- Ressonância magnética cerebral com padrão característico.
- Espectroscopia por RM — detecta lactato acumulado no cérebro durante os episódios.
A armadilha diagnóstica: o exame de sangue pode dar resultado falsamente negativo. A mutação pode estar em proporção baixa no sangue, mas em proporção muito maior no músculo ou na urina. Em 87% dos casos pediátricos revisados na literatura, a heteroplasmia em tecidos diferentes do sangue era mais alta. Isso significa que um resultado negativo, quando a suspeita clínica é forte, não descarta o diagnóstico — e o médico deve solicitar teste em urina ou considerar biópsia muscular.
A neuroimagem: o padrão que diferencia MELAS do AVC
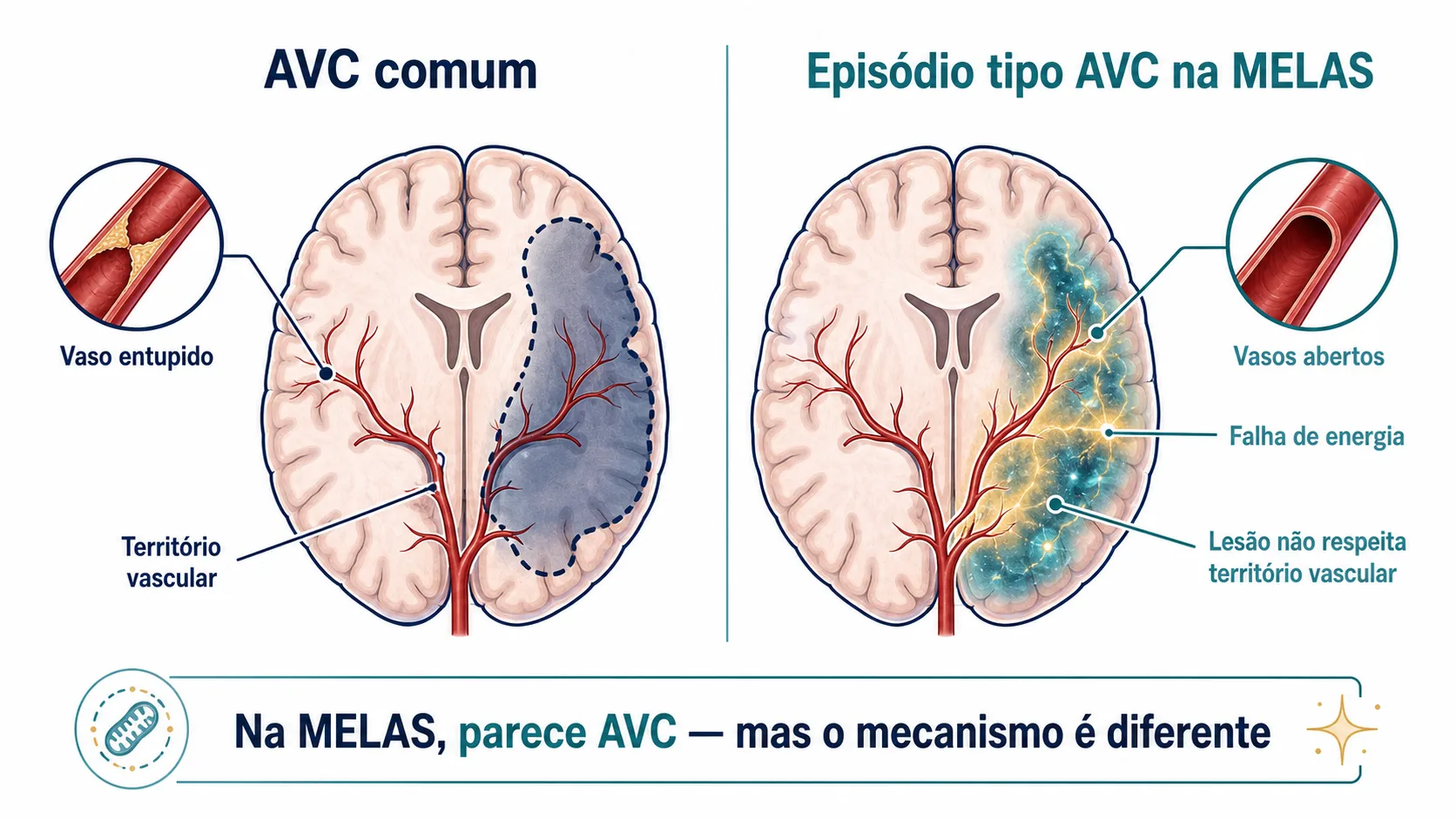
A ressonância magnética é o exame que mais ajuda a diferenciar MELAS de AVC convencional — mas apenas se quem interpreta conhecer o padrão específico da doença.
O que se vê no AVC: lesão em território vascular definido (como a área irrigada pela artéria cerebral média), que permanece e não migra.
O que se vê na MELAS:
- Lesões que não respeitam territórios vasculares — afetam áreas que normalmente não são irrigadas por um único vaso.
- Predominância nos lobos occipital, parietal posterior e temporal (regiões de alta demanda energética).
- Lesões que podem desaparecer e reaparecer em outros locais semanas depois.
- Durante a crise: hiperperfusão (excesso de sangue) — o oposto do AVC, que tem hipoperfusão.
- Com o tempo: atrofia cerebral progressiva, lesões crônicas irreversíveis (necrose laminar cortical).
Um estudo do Children's Hospital of Philadelphia com 35 pacientes identificou dois padrões imagiológicos distintos:
| Característica | MELAS Clássica | MELAS Atípica |
|---|---|---|
| Primeira crise | Após os 10 anos | Antes dos 10 anos |
| Tamanho das lesões | Grandes (≥30 mm), posteriores | Pequenas, espalhadas, anteriores ou cerebelar |
| Surdez sensorioneural | Frequente | Rara |
| Atraso do desenvolvimento | Raramente | Frequente |
| Mutação predominante | m.3243A>G | Genes de subunidades da cadeia respiratória |
| Prognóstico | Moderado | Pior — mais falência respiratória |
Essa distinção não é apenas acadêmica: o perfil atípico tem evolução mais grave e exige monitoramento mais intensivo.
🧪 Teste rápido
Pergunta: Por que um médico de pronto-socorro pode confundir MELAS com AVC?
Resposta: Porque os sintomas são quase idênticos — confusão, perda de visão, fraqueza — e a ressonância pode mostrar uma "mancha" no cérebro. A diferença está no padrão: na MELAS, a lesão não segue o território de um único vaso, aparece com hiperperfusão e pode desaparecer. Sem conhecimento específico da doença, o padrão passa despercebido.
O que isso muda na prática?
Na prática, isso significa que qualquer episódio neurológico agudo em paciente com MELAS — ou com suspeita da doença — deve ser tratado em centro com experiência em doenças mitocondriais, se possível.
Na crise aguda, a L-arginina intravenosa deve ser administrada nas primeiras 3 horas do início dos sintomas, pois estudos mostram melhora significativa da cefaleia, alteração de consciência, distúrbio visual e fraqueza. Esse é um tratamento que o neurologista de plantão precisa conhecer.
O que observar em casa?
Anote estes sinais para relatar na próxima consulta:
- Qualquer episódio de cefaleia diferente do habitual, especialmente acompanhada de náuseas intensas.
- Alterações visuais transitórias — pontos cegos, visão turva em parte do campo, flashes.
- Episódios de fraqueza muscular assimétrica ou confusão mental, mesmo que breves e reversíveis.
- Piora progressiva da audição.
- Intolerância ao exercício desproporcional ao esforço realizado.
- Mudanças no humor, memória ou raciocínio percebidas pela família.
O que vale perguntar ao médico?
- "Meu perfil é o MELAS clássico ou atípico? Isso muda o acompanhamento?"
- "Devo fazer teste de heteroplasmia em urina além do sangue?"
- "Tenho indicação de taurina em alta dose? Qual a dose certa para meu peso?"
- "Como devo agir na crise aguda — qual pronto-socorro tem L-arginina disponível?"
- "Quais familiares devo investigar e com que frequência?"
Quando procurar ajuda mais rápido?
Vá imediatamente ao pronto-socorro se houver:
- Perda súbita de visão (parcial ou total), mesmo que transitória.
- Confusão mental ou desorientação de início abrupto.
- Convulsão (inclusive a primeira vez).
- Fraqueza súbita em um braço, perna ou metade do rosto.
- Dificuldade de falar ou entender o que outros dizem.
- Cefaleia de intensidade muito superior ao habitual ("a pior dor de cabeça da vida").
Leve sempre ao pronto-socorro um documento escrito com o diagnóstico de MELAS e a informação de que pode ser necessária L-arginina intravenosa.
Perguntas frequentes
😰 Medo
MELAS é fatal? As pessoas morrem por causa dela? MELAS é uma doença grave que pode reduzir a expectativa de vida, especialmente na forma atípica de início precoce. Porém, com tratamento adequado, muitos pacientes vivem décadas com qualidade de vida razoável. A progressão varia muito: alguns têm crises frequentes e deterioração rápida, outros ficam anos estáveis. Não há como prever o curso individual sem acompanhamento especializado.
MELAS vai piorar progressivamente ou pode estabilizar? MELAS tende a uma progressão lenta, com períodos de estabilidade intercalados por crises que causam perda neurológica cumulativa. Com tratamento preventivo — especialmente taurina e arginina — muitos pacientes conseguem longos períodos sem episódios agudos. A forma clássica tem evolução geralmente mais lenta; a forma atípica, de início na infância, tende a ser mais agressiva.
Meu filho pode ter MELAS se eu tenho a doença? MELAS é herdada pela linha materna — o DNA mitocondrial vem exclusivamente da mãe. Se você é mãe e tem MELAS, seus filhos herdarão a mutação, mas não necessariamente desenvolverão a doença completa. A gravidade depende de quantas mitocôndrias com defeito cada filho herdar, o que varia. Se você é pai com MELAS, seus filhos não herdam a mutação por essa via. Consulta com geneticista é essencial para avaliação familiar.
🏠 Dia a dia
Posso continuar trabalhando e levando uma vida normal com MELAS? Depende da gravidade e da fase da doença. Muitos pacientes com MELAS, especialmente os com forma clássica bem controlada, mantêm atividades profissionais e sociais por anos. O comprometimento cognitivo acumulado pelas crises pode limitar atividades complexas ao longo do tempo. Adaptações no trabalho e suporte multidisciplinar fazem diferença significativa na funcionalidade.
Posso dirigir tendo MELAS? Essa decisão precisa ser avaliada individualmente pelo seu neurologista, considerando se você tem histórico recente de crises, convulsões ou comprometimento visual. Em geral, pacientes com epilepsia ativa ou crises não controladas não devem dirigir. Se estiver estável há tempo suficiente, converse com seu médico sobre a liberação para dirigir — há regras específicas que variam por estado.
💊 Tratamento
Existe remédio que realmente funciona para MELAS? Sim, mas com expectativas realistas. Não existe cura, mas tratamentos que funcionam para reduzir crises. A taurina em alta dose teve um ensaio clínico Fase III japonês em que 60 em cada 100 pacientes ficaram sem nenhuma crise durante o tratamento de um ano. A L-arginina intravenosa, usada nas crises agudas, melhora os sintomas rapidamente na maioria dos casos. O chamado coquetel mitocondrial de suporte ajuda a manter a função residual das mitocôndrias.
A taurina que vende em farmácia é a mesma que trata MELAS? Não exatamente. A taurina usada nos estudos para MELAS é em dose muito alta — 9 a 12 gramas por dia para adultos, muito acima dos suplementos comuns. As doses de suplemento de venda livre (geralmente 500 mg a 1 g) são insuficientes para o efeito terapêutico documentado. O uso terapêutico deve ser prescrito e monitorado por neurologista especializado.
O coquetel mitocondrial é necessário para todos os pacientes? Não existe uma prescrição única. O coquetel — combinação de coenzima Q10, vitaminas do complexo B, vitamina E, ácido lipoico e outros — é ajustado conforme o perfil genético, os sintomas e os exames laboratoriais de cada paciente. Alguns componentes têm evidência mais sólida (ubiquinol, vitamina E, NAC em pacientes com glutationa baixa); outros são prescritos empiricamente. Vitamina C e L-carnitina, antes usadas rotineiramente, hoje não são mais recomendadas para MELAS.
🔮 Futuro
MELAS tem cura? O que a ciência está desenvolvendo? Não há cura estabelecida ainda. O horizonte mais promissor é a terapia gênica — técnicas que editam o DNA mitocondrial para reduzir a proporção de cópias defeituosas. Estudos em animais são encorajadores, mas ainda não chegaram a ensaios clínicos em larga escala para MELAS. A terapia de reposição mitocondrial, usada para prevenir a transmissão para filhos de mães afetadas, já está em ensaios humanos em alguns países.
O que esperar a longo prazo com diagnóstico de MELAS? O prognóstico varia muito pelo perfil (clássico vs. atípico), pelo tratamento recebido e pela adesão ao acompanhamento. Pacientes com diagnóstico precoce, acompanhamento multidisciplinar e tratamento adequado com arginina e taurina têm perspectiva significativamente melhor do que pacientes sem diagnóstico ou mal tratados. A progressão da perda cognitiva pode ser desacelerada com bom controle das crises.
✋ Ação
O exame genético de sangue pode dar negativo mesmo eu tendo MELAS? Sim, e isso é um ponto crítico. A mutação pode estar presente em proporção baixa no sangue mas em proporção muito maior no músculo ou urina. Um resultado negativo no sangue não exclui o diagnóstico quando a suspeita clínica é forte. Nesses casos, seu médico pode solicitar teste em amostra de urina ou biópsia muscular.
O que devo fazer se alguém com MELAS tiver uma crise em casa? Em caso de crise aguda — confusão mental, perda de visão, fraqueza súbita, convulsão — ligue imediatamente para o SAMU (192) ou vá ao pronto-socorro mais próximo. Informe a equipe que a pessoa tem MELAS e pode precisar de L-arginina intravenosa nas primeiras 3 horas do início dos sintomas. Nunca administre medicamentos por conta própria. Idealmente, o paciente deve ter um plano de crise documentado, elaborado com seu neurologista.
O que posso fazer a partir de agora?
✅ Observe: anote qualquer episódio de cefaleia intensa, alteração visual transitória, fraqueza assimétrica ou confusão mental — mesmo que curto e reversível. Leve o registro para a consulta.
✅ Pergunte ao médico: "Meu exame de heteroplasmia foi feito em sangue, urina e músculo?", "Tenho indicação de taurina em alta dose?", "Como devo agir na próxima crise?"
✅ Faça: mantenha o acompanhamento multidisciplinar regular — cardiologista, nefrologista, endocrinologista e audiólogo, além do neurologista. Mesmo sem sintomas ativos, complicações silenciosas são comuns.
❌ Não faça: não interrompa os suplementos prescritos sem orientação médica. Não tome L-carnitina ou vitamina C por conta própria — ambas podem ser prejudiciais em MELAS. Não tente usar taurina em dosagem de suplemento achando que terá o mesmo efeito do tratamento clínico.
📞 Procure ajuda rápida se: perder parte da visão de forma súbita, tiver confusão mental de início abrupto, convulsão, fraqueza intensa num lado do corpo ou cefaleia muito diferente do habitual. Esses são os sinais de um episódio agudo de MELAS — as primeiras 3 horas são a janela terapêutica crítica.
O que estes estudos NÃO provam?
- Os tratamentos descritos — em especial a taurina — foram avaliados em estudos pequenos, sem grupo placebo. Os resultados são promissores, mas não definitivos para toda a população com MELAS.
- Não está comprovado que todos os pacientes com a mutação m.3243A>G respondem da mesma forma às intervenções: o perfil genético, o nível de heteroplasmia e o órgão predominantemente afetado influenciam a resposta.
- A identificação de dois fenótipos (clássico e atípico) foi feita em 35 pacientes num único centro; precisa de validação em estudos maiores e multicêntricos.
- Os estudos não comprovam que o coquetel mitocondrial modifica a história natural da doença — apenas que é geralmente seguro e razoável do ponto de vista bioquímico.
- Nenhum dos tratamentos disponíveis atua na causa genética — apenas nos mecanismos de doença. A terapia gênica, que poderia ser modificadora da causa, ainda está em fase experimental.
⚕️ IMPORTANTE Este conteúdo reúne e explica informações de estudos científicos publicados e não substitui a consulta médica. Se você ou um familiar tem sintomas descritos aqui, converse com um neurologista. Não interrompa nem inicie medicamentos ou suplementos por conta própria. Cada pessoa é única — o que vale para os grupos estudados pode não se aplicar ao seu caso específico.
Referências científicas:
NA, Ji-Hoon; LEE, Young-Mock. Diagnosis and management of mitochondrial encephalopathy, lactic acidosis, and stroke-like episodes syndrome. Biomolecules, Basel, v. 14, n. 12, p. 1524, dez. 2024. DOI: 10.3390/biom14121524.
BARCELOS, Isabella et al. Mitochondrial medicine therapies: rationale, evidence, and dosing guidelines. Current Opinion in Pediatrics, Philadelphia, v. 32, n. 6, p. 707–718, dez. 2020. DOI: 10.1097/MOP.0000000000000954.
ALVES, Cesar A. P. F. et al. MELAS: phenotype classification into classic-versus-atypical presentations. AJNR American Journal of Neuroradiology, Oak Brook, v. 44, n. 5, p. 602–610, maio 2023. DOI: 10.3174/ajnr.A7837.
SEED, Lydia M. et al. Molecular and neurological features of MELAS syndrome in paediatric patients: a case series and review of the literature. Molecular Genetics & Genomic Medicine, Hoboken, v. 10, n. 6, e1955, jun. 2022. DOI: 10.1002/mgg3.1955.
TETSUKA, Syuichi et al. Clinical features, pathogenesis, and management of stroke-like episodes due to MELAS. Metabolic Brain Disease, New York, v. 36, n. 8, p. 2181–2193, dez. 2021. DOI: 10.1007/s11011-021-00772-x.
✍️ Dr. Thiago G. Guimarães Médico Neurologista | CRM-SP 178.347 Especialista em Distúrbios do Movimento e Neurogenética Hospital das Clínicas da FMUSP
📍 Consultório: Rua Cristiano Viana, 328 – Conj. 201 – Pinheiros, São Paulo/SP 🎬 YouTube: youtube.com/@DrThiagoGGuimaraes 📸 Instagram: @dr.thiagogguimaraes.neuro 🌐 Site: drthiagoguimaraesneuro.com
Este conteúdo tem finalidade educativa e não substitui a consulta médica.
Artigos Relacionados
Selecionamos outros conteúdos sobre o mesmo tema para aprofundar a leitura de forma prática e organizada.

Ataxia de Friedreich de início tardio: quando a doença aparece só na vida adulta
A ataxia de Friedreich pode começar após os 25, 40 ou até 60 anos. Entenda os sinais, por que o diagnóstico pode ser confundido e quando pensar em teste genético.

Charcot-Marie-Tooth: diagnóstico, genética e tratamento da neuropatia hereditária mais comum
Entenda a doença de Charcot-Marie-Tooth, uma neuropatia hereditária que afeta nervos dos pés, pernas e mãos. Saiba como é feito o diagnóstico, quando pedir teste genético e quais tratamentos ajudam na prática.

Omaveloxolona na ataxia de Friedreich: quais benefícios esperar e quais limites entender
Entenda, em linguagem simples, o que os estudos MOXIe mostraram sobre a omaveloxolona na ataxia de Friedreich: benefícios potenciais, segurança, limitações e perguntas para levar ao neurologista.

SCA27B e o sinal do pedúnculo cerebelar superior na ressonância
Entenda como um achado de ressonância chamado sinal do trato do pedúnculo cerebelar superior pode ajudar a levantar suspeita de SCA27B, uma forma de ataxia cerebelar de início tardio ligada ao gene FGF14.
Agende sua Consulta
Discuta seu caso com o Dr. Thiago G. Guimarães, neurologista formado pela USP, especialista em Distúrbios do Movimento e Neurogenética. Atendimento presencial em São Paulo ou por telemedicina.
📍 Consultório: R. Cristiano Viana, 328 - Conj. 201, Pinheiros, São Paulo/SP